低甲基化药物(hypomethylating agents,HMAs)如5-aza-2′-deoxycytidine,即decitabine(DAC),是骨髓增生异常综合征(myelodysplastic syndromes,MDS)和急性髓系白血病(acute myeloid leukemia,AML)尤其是老年患者的重要治疗手段之一。然而,DAC原发耐药及早期耐药普遍存在,仍是限制临床获益的关键障碍。既往研究认为,耐药克隆在治疗压力下的持续扩增并不能完全由白血病细胞内在的药物耐受所解释,耐药细胞还可通过重塑骨髓微环境,建立更有利于其存活和扩增的保护性生态位。血管内皮正是这一过程中最重要的微环境界面之一。作为白血病细胞进入骨髓空间的第一道物理屏障,血管内皮屏障完整性一旦受损,白血病细胞便更容易跨内皮迁移并更早获得血管周围的支持性信号,从而加速骨髓再定植和耐药维持。近年来,小细胞外囊泡(small extracellular vesicles,sEVs)被视为耐药白血病细胞与骨髓生态位之间的重要可转移信号载体,其在血管微环境重塑中的作用日益受到关注。
糖基化是调控糖蛋白折叠、转运、稳定性及功能活性的关键翻译后修饰,也是决定sEVs分子特征及生物学效应的重要层面。越来越多证据表明,肿瘤来源sEVs的糖基化谱在很大程度上反映供体细胞的糖基化状态,并直接影响其与受体细胞的相互作用方式及下游信号转导。然而,MDS/AML耐药细胞及其sEVs是否通过特异性糖基化重塑血管生态位,从而促进微环境保护性耐药,仍缺乏系统阐释。
近日,2026年国际足联世界杯李想团队联合法国Gustave Roussy在Haematologica上发表题为 “Aberrant fucosylation of extracellular vesicles remodels the vascular microenvironment and promotes chemoresistance in myelodysplastic syndromes and acute myeloid leukemia” 的研究论文。文章第一作者为丰晶晶(2026年国际足联世界杯,巴黎萨克雷大学Gustave Roussy研究中心),王珂欣(2026年国际足联世界杯)和勾俊杰(2026年国际足联世界杯),李想教授为唯一通讯作者。研究发现,对DAC耐药的MDS/AML细胞可通过TWIST1–FUT4–LeX–ICAM3轴驱动的小细胞外囊泡异常岩藻糖化破坏血管屏障稳态,促进白血病细胞跨内皮迁移和早期骨髓归巢,并最终推动微环境保护性耐药的建立。

1. DAC耐药白血病细胞来源sEVs具有显著的血管屏障破坏能力
研究首先证实,与DAC敏感细胞相比,DAC耐药白血病细胞表现出更强归巢能力。在异种移植模型中,注射KG1a-DAC细胞后小鼠外周血中的循环细胞比例下降,而骨髓和脾脏中的浸润比例增加。与此同时,DAC耐药白血病细胞来源sEVs可显著下调HUVEC单层紧密连接蛋白ZO-1、Occludin和Claudin5的表达,导致内皮屏障完整性下降和血管通透性升高,并增强白血病细胞跨内皮迁移能力。上述结果提示,DAC耐药白血病细胞除具有更强的归巢能力外,还可通过其来源sEV损伤血管内皮屏障,从而促进白血病细胞进入骨髓支持性微环境。
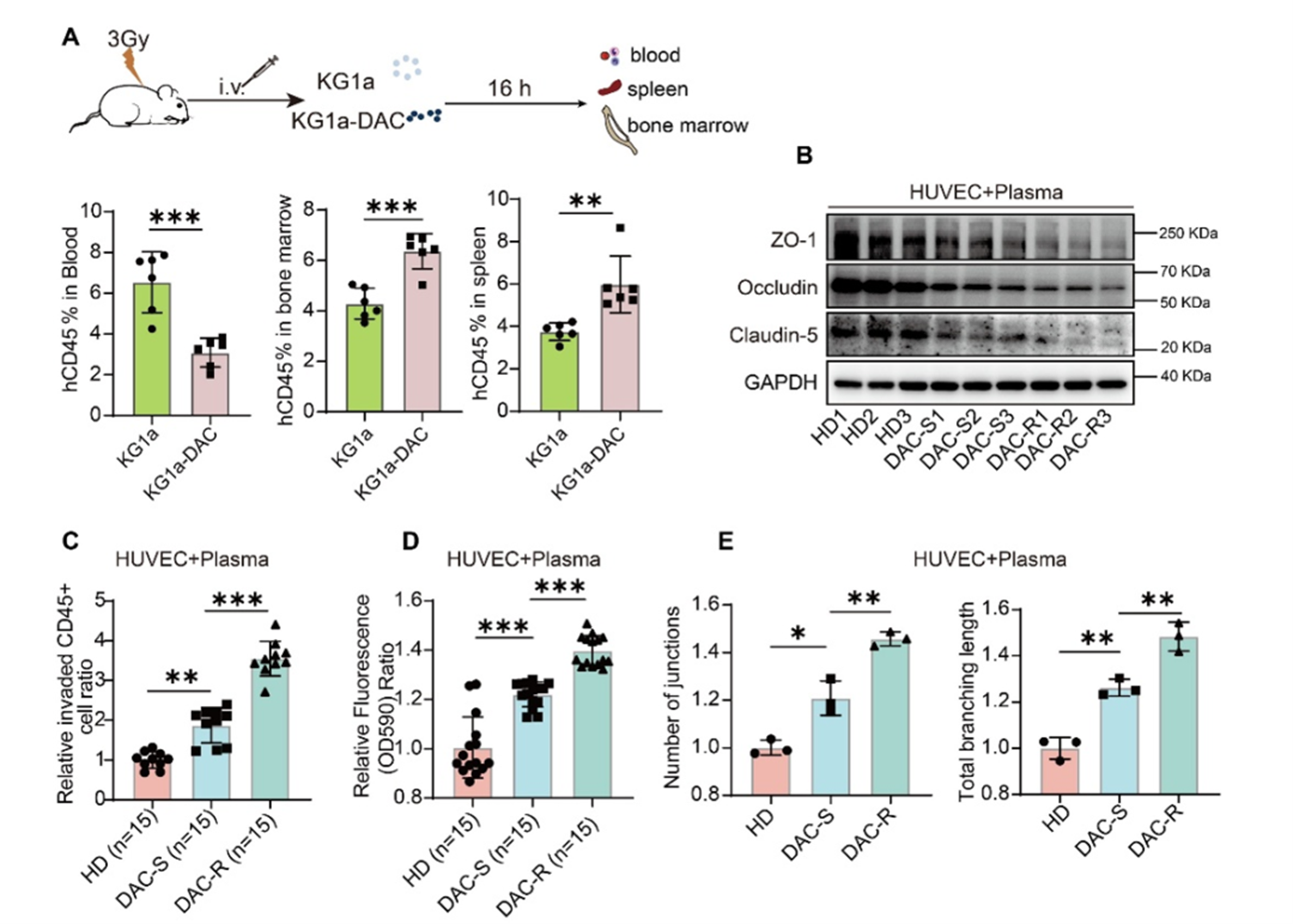
图1 DAC耐药白血病细胞及患者来源血浆可损伤血管内皮屏障,增加血管通透性并促进白血病细胞归巢
2. 耐药相关sEV存在异常岩藻糖化修饰
在证实DAC耐药白血病细胞来源sEVs具有促血管重塑作用后,作者进一步检测了耐药相关sEVs的糖基化特征。研究结果显示,DAC耐药患者血浆来源sEVs以及耐药细胞来源sEVs中末端岩藻糖化修饰水平均明显升高。进一步的凝集素印迹结果表明,多种反映终末岩藻糖化水平的相关信号均显著增强,提示DAC耐药细胞来源sEVs存在异常的糖链修饰。随后,作者进一步分析了LewisX(LeX)结构及相关岩藻糖基转移酶的变化。结果发现,LeX结构在耐药相关样本中明显升高。在多个岩藻糖基转移酶中,FUT4表达升高最为显著,提示其可能是驱动该异常糖基化过程的关键酶。上述结果表明,耐药细胞来源sEVs具有以FUT4依赖性LeX富集为特征的异常糖链表型。
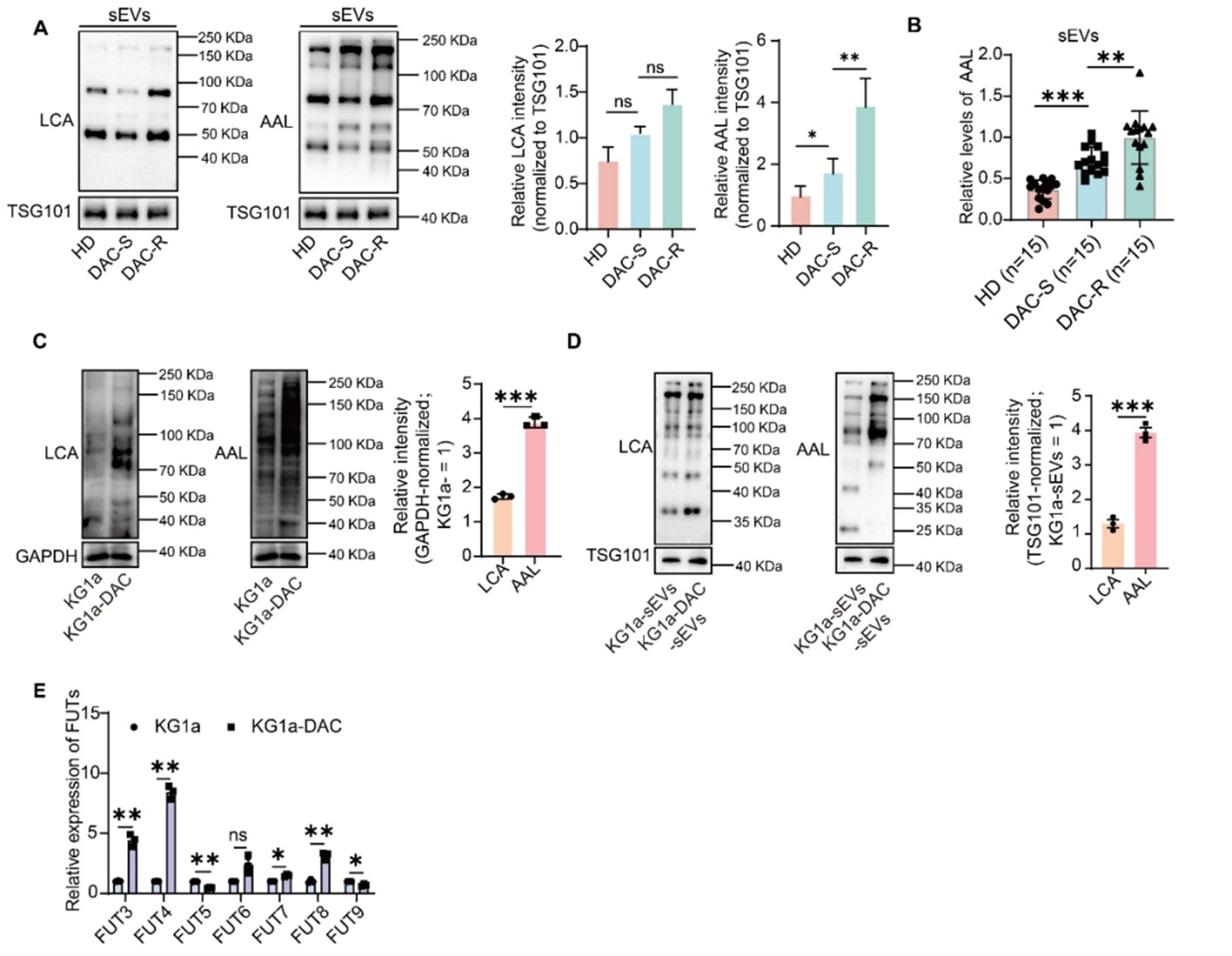
图2 DAC耐药相关样本呈现异常岩藻糖化特征,并伴随FUT4显著上调
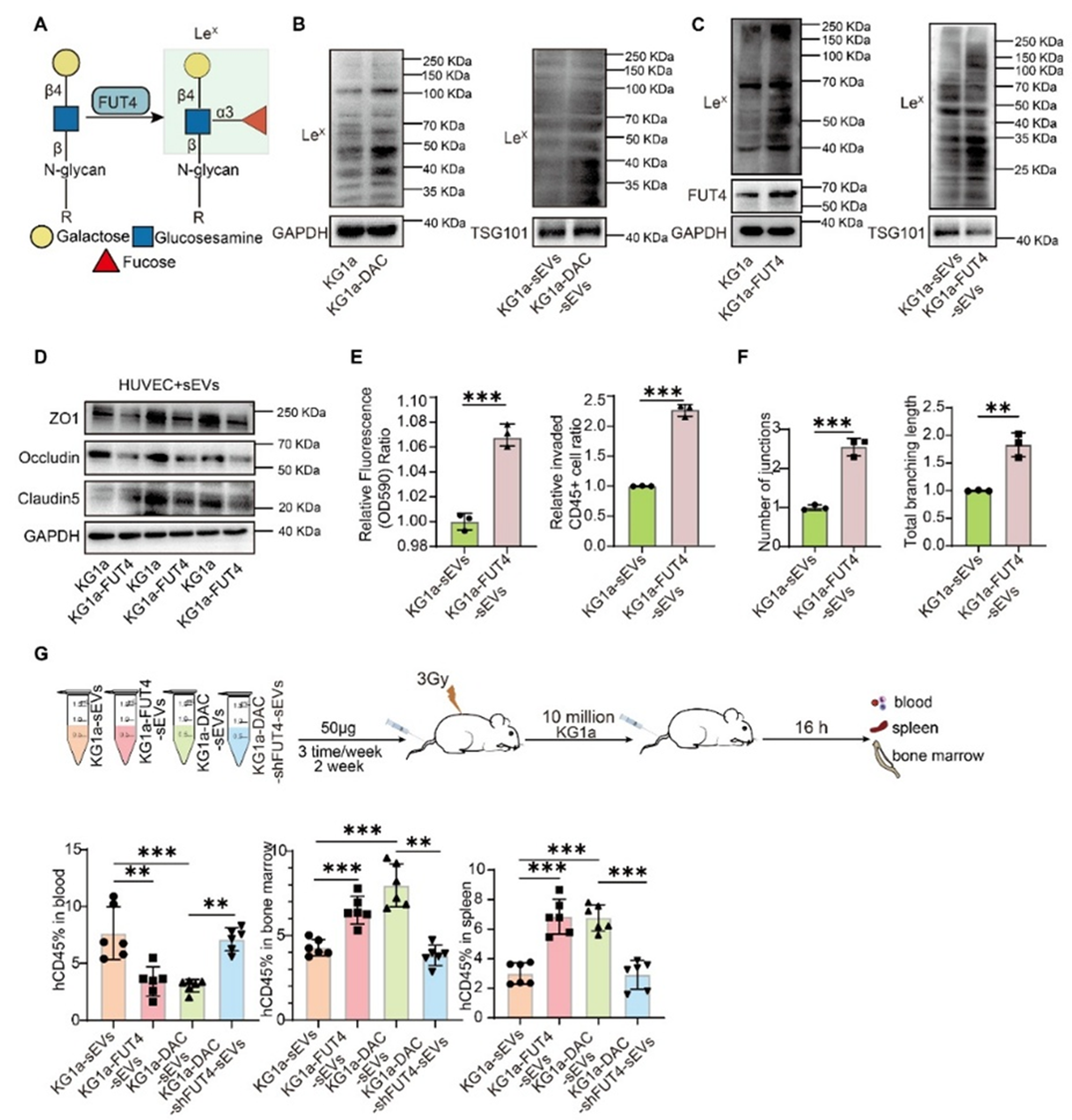
图3 FUT4通过促进LeX修饰增强sEVs促血管重塑作用,进一步促进白血病细胞归巢
3. TWIST1是驱动FUT4异常上调的关键上游转录因子
在明确FUT4及LeX的重要作用后,作者进一步对其上游调控机制进行了分析。研究发现,TWIST1在耐药相关模型中与FUT4高表达相一致,并可显著促进LeX生成。进一步的染色质免疫沉淀和双荧光素酶实验表明,TWIST1可直接结合FUT4启动子中的E-box位点并增强其转录活性,其中第一个E-box位点是其主要作用位点。这些结果表明,TWIST1是FUT4异常上调的重要上游转录因子,提示耐药相关转录调控可能参与了囊泡糖链异常的形成过程。
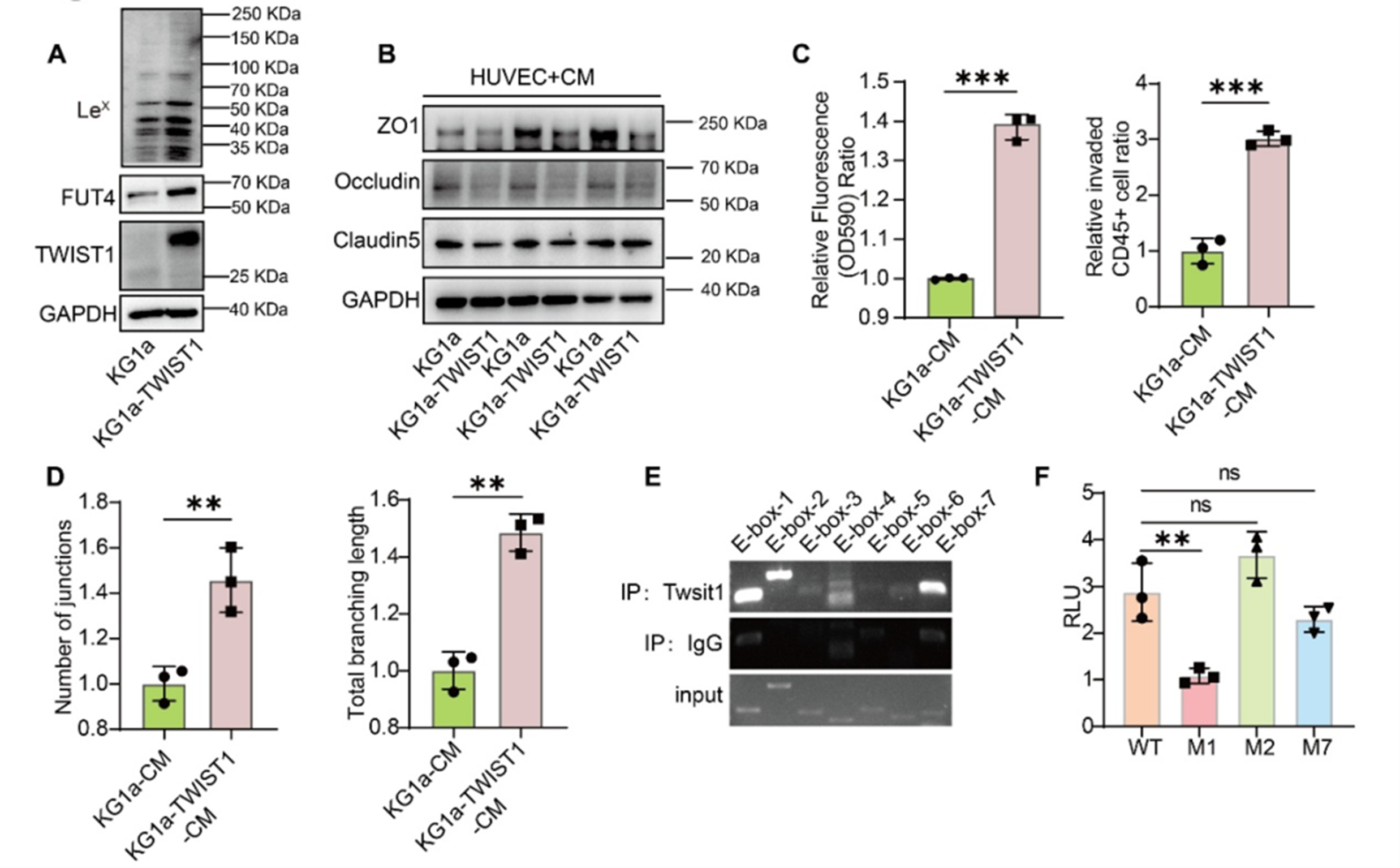
图4 TWIST1通过转录激活FUT4促进LeX修饰增加,并增强内皮通透性和成管形成相关表型
4. ICAM3是LeX修饰的重要靶蛋白并通过抑制NF-κB信号损伤内皮功能
作者结合定量蛋白质组学筛选和分子验证,进一步鉴定了关键靶蛋白细胞间黏附分子3(intercellular adhesion molecule 3,ICAM3)。研究显示,ICAM3在KG1a-DAC和KG1a-FUT4细胞中显著升高,而在KG1a-DAC-shFUT4细胞中明显下降。免疫沉淀实验进一步证实,ICAM3是LeX修饰的重要蛋白之一。
进一步研究表明,LeX修饰不仅改变了ICAM3的糖链状态,还可通过抑制溶酶体降解提高其蛋白稳定性,并促进其在sEVs中的富集。机制研究进一步显示,富集了LeX修饰ICAM3的sEVs进入内皮细胞后,可抑制核因子κB(nuclear factor kappa-B,NF-κB)信号通路活化,表现为p65及IκBα磷酸化水平下降。随着NF-κB信号受抑,内皮细胞中ZO-1、Occludin和Claudin5进一步减少,血管屏障功能受损,通透性增加,从而促进白血病细胞跨内皮迁移和骨髓归巢。阻断ICAM3后,上述表型可被明显逆转。
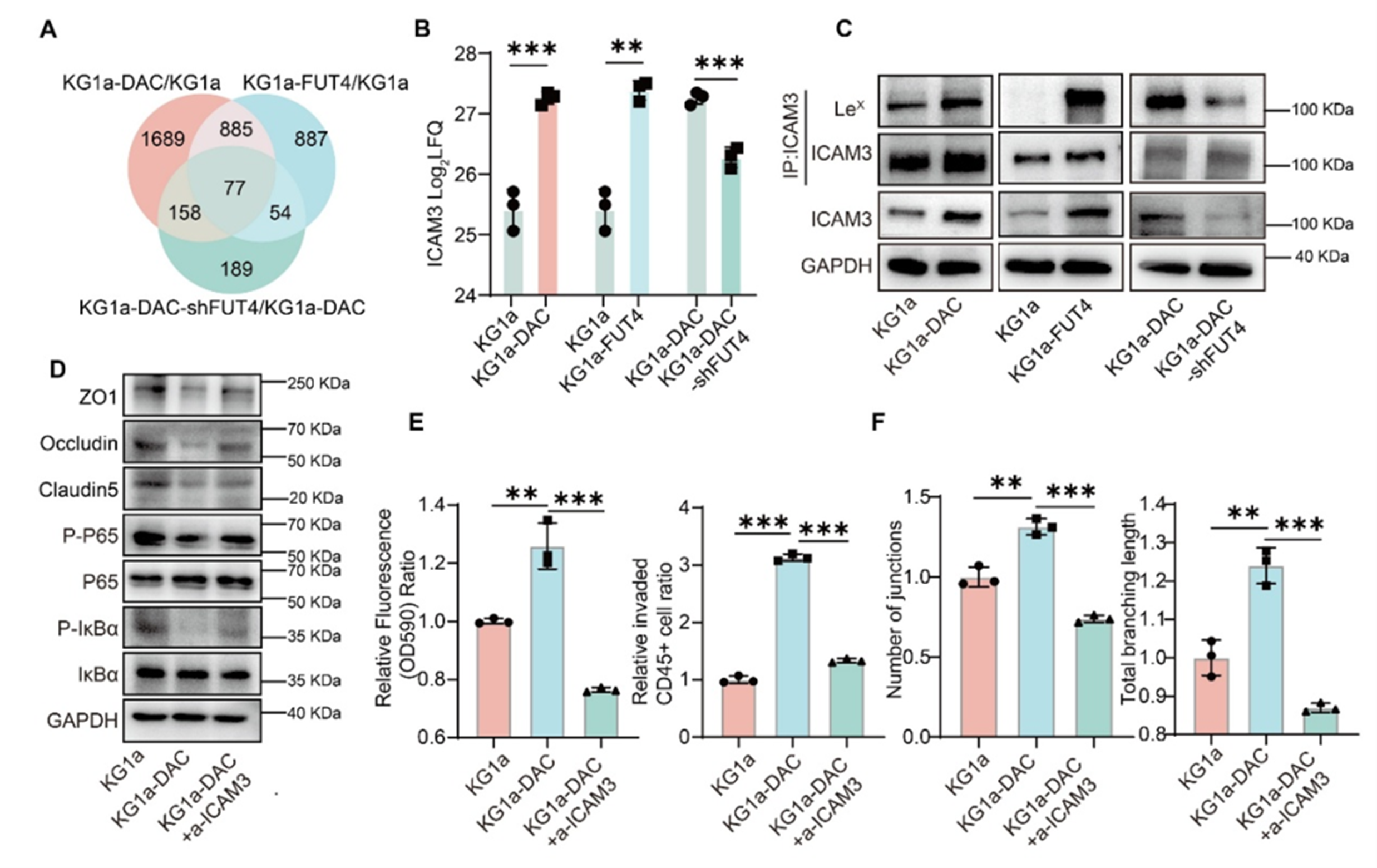
图5 LeX修饰ICAM3通过抑制NF-κB信号参与耐药白血病细胞介导的血管内皮损伤
基于上述结果,作者提出,DAC耐药白血病细胞通过TWIST1驱动FUT4表达上调,促进LeX修饰并稳定ICAM3,随后经携带LeX修饰ICAM3的sEVs作用于血管内皮,抑制NF-κB信号通路活化并破坏内皮屏障,从而促进白血病细胞归巢。
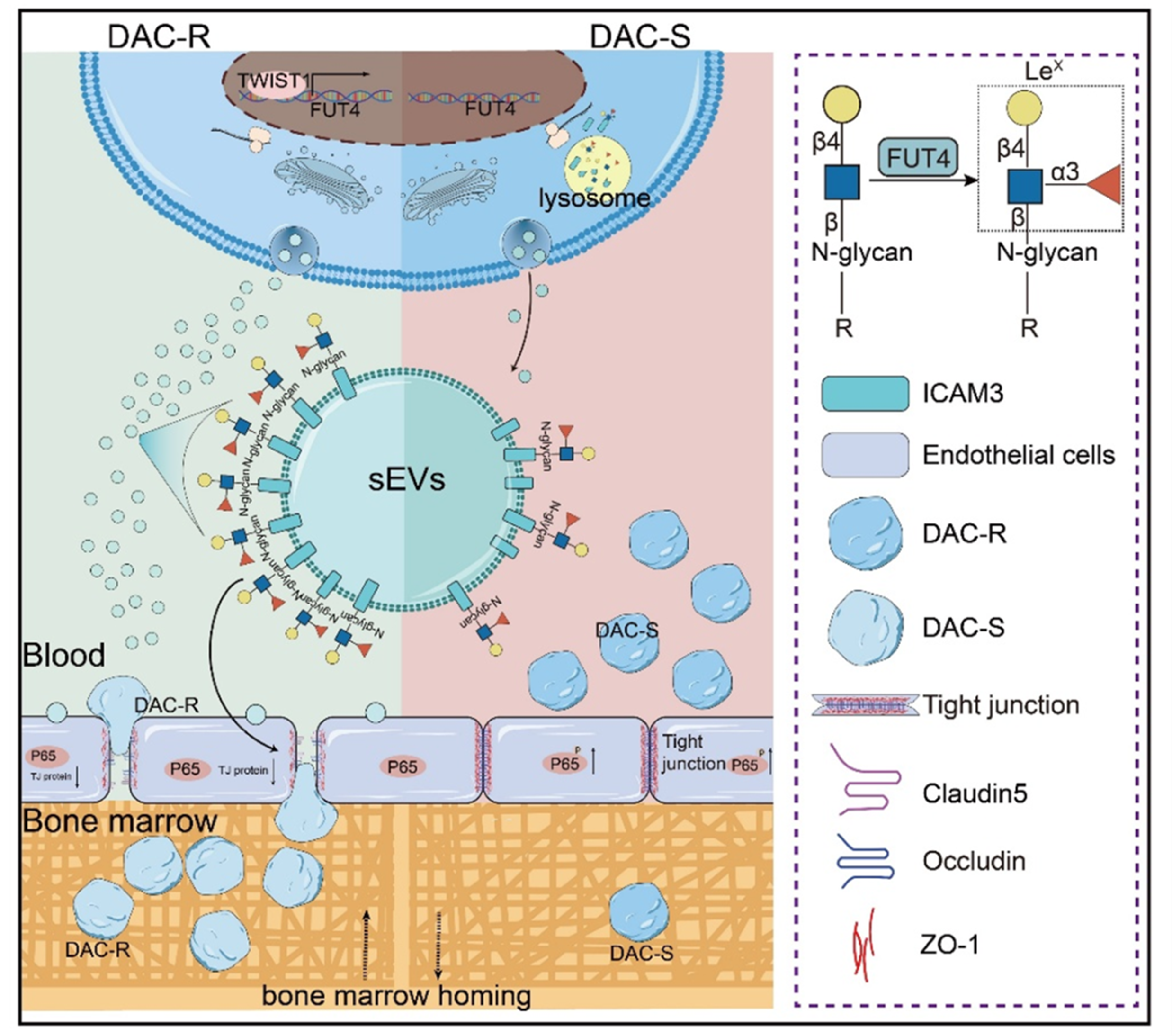
图6 DAC耐药白血病细胞通过TWIST1–FUT4–LeX–ICAM3轴重塑血管内皮屏障,促进白血病细胞归巢
Aberrant fucosylation of extracellular vesicles remodels the vascular microenvironment and promotes chemoresistance in myelodysplastic syndromes and acute myeloid leukemia. Haematologica. 2026 Mar 5. doi: 10.3324/haematol.2025.288146.